Denken: Onder normale fysiologische omstandigheden
1. Waarom stolt het bloed dat door de bloedvaten stroomt niet?
2. Waarom kan een beschadigd bloedvat na een trauma stoppen met bloeden?
Met bovenstaande vragen beginnen we vandaag aan de cursus!
Onder normale fysiologische omstandigheden stroomt bloed door de bloedvaten en zal het niet buiten de bloedvaten stromen om bloedingen te veroorzaken, noch zal het in de bloedvaten stollen en trombose veroorzaken. De belangrijkste reden hiervoor is dat het menselijk lichaam beschikt over complexe en perfecte hemostase- en antistollingsfuncties. Wanneer deze functie verstoord is, loopt het lichaam risico op bloedingen of trombose.
1. Hemostaseproces
We weten allemaal dat het hemostaseproces in het menselijk lichaam eerst bestaat uit het samentrekken van de bloedvaten, gevolgd door de hechting, samenklontering en afgifte van verschillende procoagulerende stoffen door bloedplaatjes, waardoor zachte bloedplaatjesembolieën ontstaan. Dit proces wordt eenstapshemostase genoemd.
Belangrijker nog is echter dat het het stollingssysteem activeert, een fibrinenetwerk vormt en uiteindelijk een stabiele trombus creëert. Dit proces wordt secundaire hemostase genoemd.
2. Stollingsmechanisme
Bloedstolling is een proces waarbij stollingsfactoren in een bepaalde volgorde worden geactiveerd om trombine te genereren, waarna fibrinogeen uiteindelijk wordt omgezet in fibrine. Het stollingsproces kan worden onderverdeeld in drie basisstappen: de vorming van het protrombinasecomplex, de activering van trombine en de productie van fibrine.
Stollingsfactoren is de verzamelnaam voor stoffen die rechtstreeks betrokken zijn bij de bloedstolling in plasma en weefsels. Momenteel zijn er 12 stollingsfactoren, aangeduid met Romeinse cijfers, namelijk stollingsfactoren I t/m X III (VI wordt niet langer beschouwd als een onafhankelijke stollingsfactor), met uitzondering van IV, die in ionische vorm voorkomt; de rest zijn eiwitten. De productie van II, VI, VI en III vereist de deelname van vitamine K.
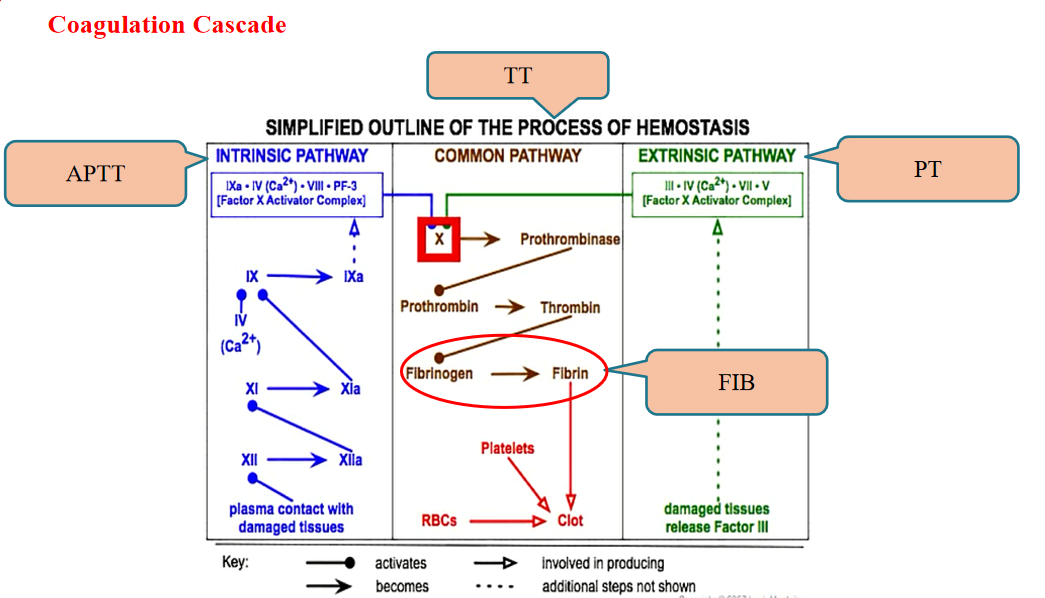
Afhankelijk van de verschillende initiatiemethoden en de betrokken stollingsfactoren kunnen de routes voor het genereren van protrombinasecomplexen worden onderverdeeld in endogene en exogene stollingsroutes.
Het endogene bloedstollingsproces (veelgebruikte APTT-test) houdt in dat alle factoren die bij de bloedstolling betrokken zijn, afkomstig zijn uit het bloed zelf. Dit proces wordt meestal op gang gebracht door het contact van het bloed met een negatief geladen vreemd lichaam (zoals glas, kaolien, collageen, enz.). Het stollingsproces dat wordt geïnitieerd door blootstelling aan weefselfactor wordt het exogene stollingsproces genoemd (veelgebruikte PT-test).
Wanneer het lichaam zich in een pathologische toestand bevindt, kunnen bacteriële endotoxinen, complement C5a, immuuncomplexen, tumornecrosefactor, enz. vasculaire endotheelcellen en monocyten stimuleren om weefselfactor tot expressie te brengen, waardoor het stollingsproces wordt geïnitieerd en diffuse intravasculaire stolling (DIC) ontstaat.
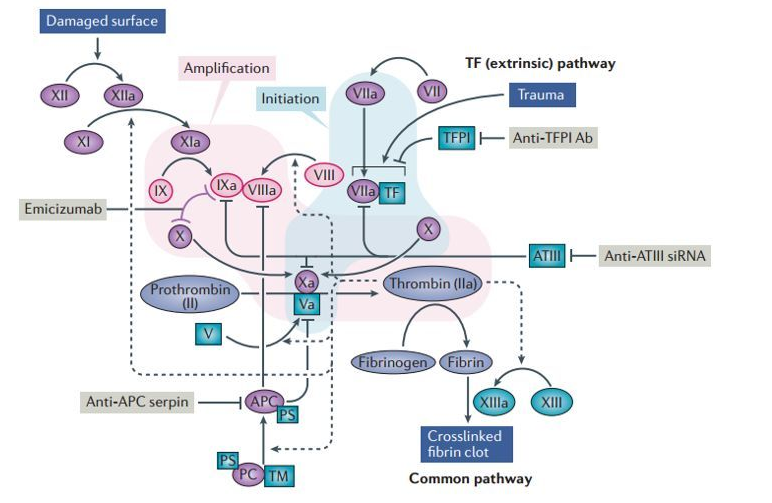
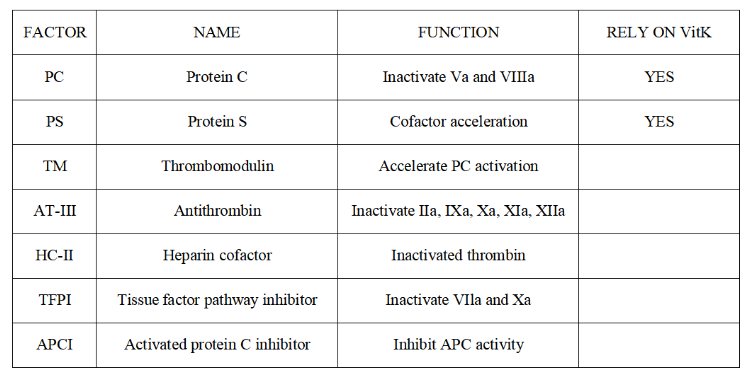
3. Anticoagulatiemechanisme
a. Antitrombinesysteem (AT, HC-II)
b. Eiwit C-systeem (PC, PS, TM)
c. Weefselfactor-pathway-remmer (TFPI)
Functie: Vermindert de vorming van fibrine en verlaagt de activatiegraad van diverse stollingsfactoren.
4. Fibrinolytisch mechanisme
Wanneer bloed stolt, wordt PLG geactiveerd tot PL onder invloed van t-PA of u-PA, wat de afbraak van fibrine bevordert en fibrine(proto)afbraakproducten (FDP) vormt. Het cross-linked fibrine wordt afgebroken tot een specifiek product, D-dimeer genaamd. De activering van het fibrinolytische systeem is hoofdzakelijk onderverdeeld in een interne activeringsroute, een externe activeringsroute en een externe activeringsroute.
Interne activeringsroute: Dit is de route waarlangs PL wordt gevormd door de splitsing van PLG door de endogene stollingsroute, wat de theoretische basis vormt van secundaire fibrinolyse. Externe activeringsroute: Dit is de route waarlangs t-PA, dat vrijkomt uit vasculaire endotheelcellen, PLG splitst om PL te vormen, wat de theoretische basis vormt van primaire fibrinolyse. Exogene activeringsroute: Trombolytische geneesmiddelen zoals SK, UK en t-PA, die van buitenaf het menselijk lichaam binnenkomen, kunnen PLG activeren tot PL, wat de theoretische basis vormt van trombolytische therapie.
De mechanismen die betrokken zijn bij de stollings-, antistollings- en fibrinolyse-systemen zijn complex, en er zijn veel gerelateerde laboratoriumtests, maar waar we vooral aandacht aan moeten besteden, is het dynamische evenwicht tussen de systemen, dat niet te sterk of te zwak mag zijn.


 Visitekaartje
Visitekaartje Chinese WeChat
Chinese WeChat